Materi:
laju reaksi
Salah satu teori yang menjelaskan proses terjadinya reaksi adalah teori tumbukan. Menurut teori tumbukan, reaksi kimia terjadi karena adanya partikel-partikel yang saling bertumbukan. Tumbukan terjadi jika dua molekul atau lebih permukaannya saling bersentuhan pada satu titik. Pengertian satu titik disini adalah jika dianggap bentuk molekul bulat seperti bola, maka pada pertemuan tersebut jarak antarpusat inti sama dengan diameternya untuk jenis molekul yang mempunyai ukuran sama. Tetapi, tidak semua tumbukan akan menghasilkan reaksi kimia. Tumbukan yang dapat menghasilkan reaksi kimia dikenal dengan istilah tumbukan efektif.
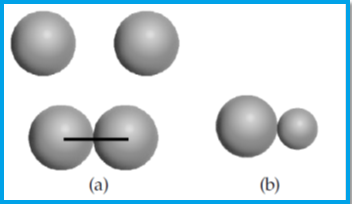
Keterangan Gambar:
(a) tumbukan molekul untuk molekul yang tidak sama
(b) tumbukan antarmolekul yang berbeda diameternya
Agar terjadi tumbukan yang efektif diperlukan syarat, yaitu orientasi tumbukan molekul harus tepat. Orientasi merupakan arah atau posisi antarmolekul yang bertumbukan. Untuk molekul berbentuk bulat orientasi tidak begitu penting, karena semua posisi akan mengakibatkan tumbukan dengan orientasi sesuai. Tetapi, untuk molekul yang berbentuk dua bola terpilin orientasi sangatlah penting.
Gambar: orientasi tumbukan
Misal tumbukan antara gas hidrogen dengan gas oksigen, seperti reaksi berikut:
Gambar: tumbukan gas hidrogen dan oksigen menghasilkan air
Selain orientasi, agar dapat terjadi reaksi kimia, maka energi tumbukan harus melewati energi penghalang yang dikenal dengan energi aktivasi. Energi aktivasi (Ea) merupakan energi minimal agar terjadi suatu reaksi. Semua proses reaksi kimia harus melalui tahap ini, jika energi aktivasi tidak terlampaui, maka reaksi kimia tidak akan terjadi. Energi aktivasi merupakan syarat minimal terjadinya suatu reaksi dan dapat digambarkan sebagai berikut:
Gambar: diagram energi aktivasi
Apa yang dapat kalian simpulkan dari Gambar tersebut? Dari diagram terlihat bahwa suatu reaktan untuk dapat menjadi produk kimia harus mempunyai energi aktivasi sebesar Ea. Jika Ea tidak terlampaui, maka tidak akan dihasilkan suatu produk.
Dari diagram tersebut juga akan terlihat apa reaksi bersifat eksoterm (mengeluarkan panas) atau endoterm (menyerap panas). Reaksi bersifat eksoterm jika energi potensial dari reaktan lebih tinggi daripada energi potensial produk. Sebaliknya reaksi bersifat endoterm jika energi potensial reaktan lebih rendah daripada energi produk.
Diagram reaksi (a) eksoterm (b) endoterm
Arrhenius telah menemukan hubungan antara energi aktivasi dengan tetapan laju reaksi. Persamaan Arrhenius tersebut secara matematika dapat dituliskan sebagai berikut.
$ \begin{align} k = Ae^{-E_a / RT} \end{align} $
Keterangan :
$ k $ = tetapan laju reaksi
$A $ = tetapan Arrhenius
$E_a $ = energi aktivasi (J mol$^{-1}$)
$ R $ = tetapan gas (8,3145 J mol$^{-1}$ K$^{-1}$)
$ T $ = suhu reaksi (Kelvin)
Dari persamaan tersebut faktor pra eksponen (sebelum tanda pangkat), yaitu A (tetapan Arrhenius ) merupakan faktor frekuensi. Karena hubungan antara tetapan kecepatan reaksi dengan faktor frekuensi tumbukan berbanding lurus, maka frekuensi tumbukan sangat mempengaruhi laju reaksi. Jika frekuensi tumbukan semakin tinggi, maka reaksi akan berjalan semakin cepat.
Demikian pembahasan materi Teori Tumbukan dan contoh-contohnya.




Tidak ada komentar:
Posting Komentar